ライソゾーム病
当院で掲載している希少難治性疾患に関する説明は、患者さん並びにご家族の皆様に参考となる情報提供であり、その検査や治療は当院では行っておりません。
また、紹介すべき病院に関しても適切な情報を持ち合わせておりません。
尚、当院では希少難治性疾患に対する医療相談は行っておりませんので、ご理解のほど宜しくお願いします。
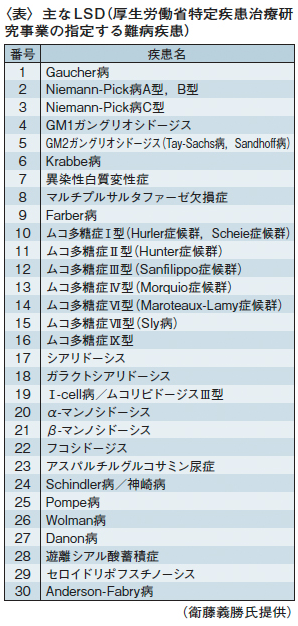
ライソゾーム病(lysosomal strage disease;LSD)
細胞内小器官であるライソゾームには多種類の分解酵素が含まれており、細胞内の蛋白質・脂肪・糖などの老廃物を分解しています。ライソゾーム病(LSD)は、ライソゾーム内の種々な加水分解酵素の先天性欠損により、代謝されるべき中間代謝産物がライソゾーム内に蓄積して種々の症状を呈する症患群です。LSDの多くは常染色体劣性遺伝性疾患で約30種類の疾患が知られており、その多くは進行性の中枢神経障害を起こし、年齢と共に症状が悪化します。脂質蓄積症、ムコ多糖症、糖原病、糖蛋白蓄積症などがあり、酵素蛋白あるいは酵素の機能発現に必要な蛋白の遺伝子変異によって生じます。多くは乳幼児期に発症しますが、成人になってから発症する病型もあります。
LSDの頻度に関する全国調査(平成13年)によると、ムコ多糖症Ⅱ型(ハンター症候群)が115例と最も多く、次いでファブリー病104例、ゴーシェ病80例、ムコ多糖症Ⅰ型(ハーラー/シャイエ症候群)37例、ポンペ病34例、ムコ多糖症Ⅳ型(モルキオ症候群)32例、セロイドリポフスチノーシス27例などの順でした。全体の頻度は、5000~6000人に1人程度と推測されています。
Gaucher病
glucocerebrosidaseの欠損によりグルコセレプロシドが肝、脾、骨髄の網内系細胞に蓄積する。1型は小児期~成人発症で肝脾腫、骨関節痛がみられるが神経症状はない。2型は乳児期発症で肝脾腫に加え、核上眼球運動障害、痙攣、知能障害を伴う.3型は1型と2型の中間型で小児期に発症し、肝脾腫、核上性眼球運動障害、運動失調、不随意運動などがみられる。
Niemann-Pick病
acid sphingomyelinase が欠損するA型、B型とNPC1蛋白の異常によって超こるC型がある。NPC1蛋白は神経系ではアストロサイトの突起内に局在し、神経細胞からのコレステロールの輸送に関係していると推測されている。スフィンゴミエリンやコレステロールが肝、脾、骨髄の網内系細胞と神経細胞に蓄積する。A型は乳児期に発症し、肝脾腫、精神運動障害や限球運動障害がみられ、B型は小児期に発症し、肝脾腫が主体であり、重症例では肺浸潤による呼吸不全を呈する.C型は発症年齢は様々で肝脾腫と核上性垂直眼球運動障害、失調、ジストニア、痴呆などの神経症状を呈する。成人発症では痴呆、抑うつ症状などの精神症状を主体とする例もある。
GM1ガングリオシドーシス
β-galactosidaseの欠損により中枢神経系にGM1ガングリオシド、骨を含む全身臓器にケラタン硫酸、オリゴ糖の蓄積が起こる。乳児型は粗な顔貌(ガルゴイリズム)、骨変形、肝脾腫、知能障害、錐体路障害、眼底にcherry red spotがみられる。若年型は症状が軽い。成人型はジストニアを主体とする錐体外路障害を呈する。
GM2ガングリオシドーシス
Tay-Sachs病はβ-hexosaminidase Aの欠損、Sandhoff病はβ-hexosaminidase A、Bの欠損、AB型はGM2活性化蛋白の欠損により、神経細胞にGM2ガングリオシドが蓄積する.乳児型は知能障害、視力障害、痙攣を呈する。若年型は運動失調、アテトーゼがみられ、成人型は脊髄小脳変性症や運動ニューロン疾患類似の症状を呈するものがある。
Globoid cell leukodystrophy(Krabbe病)
galactocerebrosidaseの欠損によりサイコシンが蓄積し、中枢と末楷神経の脱髄をきたす。ミクログリア、マクロファージがオリゴデンドログリアを貪食したものが、グロボイド細胞である。乳幼児型は精神運動障害、視神経萎縮、痙性麻痺などをきたす。成人型は痙性麻痺を呈する。
異染性白質ジストロフィー
arylsulfatase Aの欠損により脳白質、腎にスルファチドが蓄積し、中枢と末梢経神軽の脱髄をきたす。尿沈査のトルイジン青染色にて赤褐色の異染性を認める.乳幼児型は視神経萎縮、知能低下、痙性麻揮などをきたす。成人型は痴呆や精神症状が主体となる場合がある。
Multiple sulfatase欠損症
arylsulfatase Aとその他のsulfataseが欠損し、sulfataseの活性化障害があり、最近原因遺伝子も判明した。乳児期に発症し、精神運動発達遅滞、視神経萎縮、痙性麻痺などの神経症状に加え、ガルゴイリズム、肝脾腫、骨格変形といったムコ多糖症様の症候を呈する。
Farber病
セラミダーゼ酵素異常により脂質が分解されず、関節、肝、脾、心臓、腎、咽頭、中枢神経などに脂質が蓄積して症状を呈する。乳幼児から、精神発達遅滞、嚥下障害、嘔吐、さ声、黄色腫、呼吸機能低下などを伴い、2歳までに死亡する。
ムコ多糖症
ムコ多糖症I型 (Hurler/Scheie症候群)
α-iduronidaseの欠損によりデルマタン硫酸、 ヘパラン硫酸の蓄積、尿中増加を認める。乳児期から強い身体奇形(ガルゴイリズム、オール様助骨、関節拘縮、椎体変形)、知能障害があり、角膜混濁による視力障害、肝脾腫、ヘルニアなどもみられる。Scheie症候群は軽症で知能はほぼ正常である。
ムコ多糖症II型 (Hunter 症候群)
iduronate sulfataseの欠損によりデルマタン硫酸、ペバラン硫酸の蓄積、尿中増加を認める。伴性劣性遺伝である。Hurler症候群に類似するが、角膜混濁はない。成人発症例は軽症で知能は正常。
ムコ多糖症III型 (Sanfilippo 症候群)
A型heparan N-sulfatase、B型α-N-acetylglucosaminidase、 C型acetyl CoA:α-glucosaminidase acetyltransferase、D型N-acetylglucosamine 6-sulfataseの欠損こよりへパラン硫酸の蓄積、尿中増加を認める。小児期発症で、行動異常(多動粗暴)、精神運動発達遅滞、粗な髪、多毛、軽度肝脾腫(小児)、難聴、痙攣、退行がみられるが、骨格異常などの身体症状は軽い。A型が最も重症である。
ムコ多糖症IV型 (Morquio 症候群)
A型はgalactose 6-sulfataseの欠損によりケラタン碇酸、 コンドロイチン硫酸の蓄積、尿中増加を認める。B型はβ-galactosidaseの欠損によりケラタン硫酸の蓄積、尿中増加を認める。脊椎後側奪、肋骨弓突出、短胴型低身長(110cm以下)、Ⅹ脚、筋緊張低下、関節過伸展、高度の骨変形、環軸椎亜脱臼、角膜混濁、難聴、心弁膜症などがみられるが、知能は正常である。
ムコ多糖症VI型 (Maroteaux-Lamy 症候群)
N-acetylgalactosamine 4-sulfatase (arylsulfatase B)の欠損によりデルマタン硫酸の蓄積、尿中増加を認める。Hurler症候群様の体形と角膜混滞がみられるが、知能は正常である。
ムコ多糖症VII型 (Sly 病)
β-glucuronidaseの欠損によりデルマタン硫酸、 ヘバラン硫酸、 コンドロイチン硫酸の蓄積、 尿中増加を認める。ガルゴイリズム、肝脾腫、骨変形、精神運動発達遅滞がみられる。
ムコ多糖症IX型
全世界で数例の患者が報告されているのみ。
シアリドーシス
sialidase の欠損によりシアリルオリゴ糖が蓄積する.思春期発症で、cherry red spot、視力障害、白内障、ミオクローヌス、歩行障害を呈する。
ガラクトシアリドーシス
保護蛋白の異常によりsialidase とβ-galactosidase の両方が欠損する。本邦に多く、思春期に歩行障害、視力・聴力障害で発症し、cbeny red spot、小脳失調、ミオクローヌス、痙攣、骨変形、被角血管腫がみられる。
l-celI病/ムコリピドーシスIII型
UDP-N-acetylglucosamine:lysosomal enzyme N-acetyl-glucosamine-1-phosphortrans ferase の欠損により、ライソゾーム酵素のマンノース6-リン酸標識が障害され、酵素のライソゾームヘの局在が障害される。乳児期発症で、ムコ多糖症様のガルゴイリズム、骨変形、関節拘縮、巨舌、肝腫、ヘルニア、角膜混濁、重度の精神運動発達遅滞がみられるが、ムコ多糖尿はない。網内系細胞の細胞質中に多くの空胞(inclusion body)がみられる。pseudo-Hurler polydystrophy は軽症型である。
α-マンノシドーシス
α-mannosidaseの欠損により、マンノース含有オリゴ糖が蓄積する。ガルゴイリズム、精神運動発達連滞、骨変形、薙聴、ヘルニア、白内障、角膜混濁がみられる。重症乳児型と軽症の若年型がある。
β-マンノシドーシス
β-mannosidaseの欠損により、マンノース含有オリゴ糖が蓄積する。小児期発症で、精神運動発達遅滞、・被角血管腫、難聴、易感染性がみられる。
フコシドーシス
α-fucosidaseの欠損により糖脂質と糖ペプチドが蓄積する。重症乳児型(Ⅰ型)は、ガルゴイリズム、精神運動発達遅滞、肝脾腫、 心肥大、痙攣、易感染性、骨変形、汗のNaCl濃度上昇がみられ、軽症型(II型)は上記に加え被角血管腫がみられる。汗のNaCl濃度は正常である。
アスバルチルグルコサミン尿症
aspartylglucosaminidaseの欠損によりアスパルチルグルコサミンが蓄積する。フィンランドに多い。乳児期に易感染性、ヘルニアで発症し、顔貌異常は遅れて明らかとなる。学童期以後に知能低下が進行し、異常行動や興奮性がみられる。
Shindler病/神崎病
成人のびまん性被角血管腫をきたす疾患として皮膚科から報告された疾患である。欠損酵素はライソゾームにあるαNアセチルガラクトサミニデースであるが同じ欠損酵素で重篤な中枢神経病変をきたす疾患が報告されており、どのようなメカニズムどこのような違いになるかは不明である。頻度はライソゾーム病の中でも稀である。
Pompe病(糖原病II型)
グリコーゲンを分解するαグルコシダーゼの欠損により全身の臓器にグリコーゲンの蓄積する疾患で、糖原病II型とも分類されている。乳児型から成人型まである。成人型になるに従い筋弱力が中心となる。
Wolman病
acid lipaseの欠損によりコレステロールエステルやトリグリセリドが蓄積する。乳児期に発症し、肝脾腫、脂肪便、 腹部膨満、副腎の石灰化がみられる。
Danon病
ライソゾーム膜(LMPII)の異常症で、主な症状は筋弱力である。
遊離シアル酸蓄積症
遊離シアル酸がライソゾームに蓄積する疾患で、ライソゾームから遊離シアル酸を転送する機構の異常である。フィンランドのある地方に多い疾患であり、日本では稀である。
セロイドリポフスチノーシス
神経変性疾患の症候群であり様々な原因がある。退行変性をきたす疾患でライソゾーム酵素測定で除外された場合この疾患を鑑別診断に入れる必要がある。従来は電子顕微鏡による病理診断がなされていたが、現在では8種以上の遺伝子が単離され遺伝子診断が可能であるが、病型が様々であり困難である。
Fabry病
α-ガラクトシダーゼ Aの欠損によりトリヘキソシルセラミド、ジガラクトシルセラミドが蓄積する。伴性劣性遺伝をとるため患者は主に男子であるが、女性保因者も軽度の症状を呈することがある。皮膚症状(血管腫)・心症状・腎障害・末梢神経障害を呈する。
治療
以前は効果が期待できる治療法がなかったが、1990年代に酵素補充療法(ERT)が開発され、多くの疾患で症状改善や、進行抑制が明らかにされている。わが国では現在、6疾患(ゴーシェ病、ファブリー病、ハーラー/シャイエ症候群、ハンター症候群、ポンペ病、マロトミー・ラミー症候群)にERTが可能になっている。しかし、脳や神経の症状には酵素補充療法と骨髄移植はほとんど無効です。また、症状が進行した時点での治療は効果が少ないため、乳幼児からLSDの高リスクスクリーニングを行って早期に診断して治療ができるような体制が望まれます。根本的な解決策は、再生医療あるいは遺伝子治療法の開発と考えられています。
*本症は難病特定疾患に指定されているので、公費負担による医療費助成制度の対象になります。疾患毎に認定基準があり、主治医の診断に基づき都道府県に申請し認定されると、「特定疾患医療受給者証」が交付されます。制度の概要、手続き方法を参照し、申請については最寄りの保健所にご相談ください。
執筆:2011.3


